1.5. Особенности химического состава природных вод Томской области |
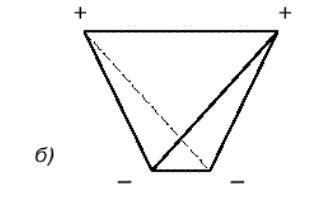
Для большей наглядности можно представить, что полюса занимают вершины деформированного тетраэдра, в центре которого находится ядро кислорода (рис. 1.1б).
Рис. 1.1б. Строение молекулы воды. Расположение полюсов заряда
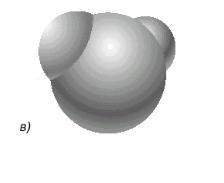
Общий вид электронного облака молекулы воды показан на рис. 1.1в.
Рис. 1.1в. Строение молекулы воды. Внешний вид электронного облака
Почти шарообразная молекула воды имеет заметно выраженную полярность, так как электрические заряды в ней расположены асимметрично. Каждая молекула воды является миниатюрным диполем с высоким дипольным моментом - 1,87 Дебая (Дебай - внесистемная единица электрического дипольного момента молекул).
Полярность молекул воды, наличие в них частично не скомпенсированных электрических зарядов порождает склонность к группировке молекул в укрупненные «сообщества» - ассоциаты.
В температурном интервале от 0 до 100°С концентрация отдельных (мономерных молекул) жидкой воды не превышает 1%. Все остальные молекулы воды объединены в ассоциаты различной степени сложности, и их состав описывается общей формулой (H2O)x.
 Непосредственной причиной образования ассоциатов являются водородные связи. Они возникают между ядрами водорода одних молекул и электронными «сгущениями» у ядер кислорода других молекул воды. Правда, эти связи в десятки раз слабее, чем «стандартные» внутримолекулярные химические связи, и достаточно обычных движений молекул, чтобы разрушить их. Но под влиянием тепловых колебаний так же легко возникают и новые связи этого типа. Возникновение и распад ассоциатов можно выразить схемой:
Непосредственной причиной образования ассоциатов являются водородные связи. Они возникают между ядрами водорода одних молекул и электронными «сгущениями» у ядер кислорода других молекул воды. Правда, эти связи в десятки раз слабее, чем «стандартные» внутримолекулярные химические связи, и достаточно обычных движений молекул, чтобы разрушить их. Но под влиянием тепловых колебаний так же легко возникают и новые связи этого типа. Возникновение и распад ассоциатов можно выразить схемой:
x H2O = (H2O)x.
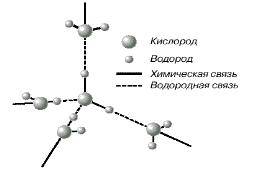
Поскольку электронные орбитали в каждой молекуле воды образуют тетраэдрическую структуру, водородные связи могут упорядочить расположение молекул воды в виде тетраэдрических координированных ассоциатов (рис. 1.2).
Рис.1.2. Схема объединения молекул воды.
Возможны и другие модели водной структуры. Тетраэдрически связанные молекулы воды образуют своеобразные рои довольно стабильного состава. Пространства между роями заполняют мономерные молекулы воды. Исследователи раскрывают все более тонкие и сложные механизмы «внутренней организации» водной массы. Кроме льдоподобной структуры, жидкой воды и мономерных молекул, описан и третий элемент не тетраэдрической структуры. Определенная часть молекул воды ассоциирована не в трехмерные каркасы, а в линейные кольцевые объединения. Кольца, группируясь, образуют еще более сложные комплексы ассоциатов. Изучение структуры жидкой воды еще незакончено; оно дает все новые факты, углубляя и усложняя наши представления об окружающем мире.
Развитие этих представлений помогает понять многие аномальные свойства воды и особенности взаимодействия ее, как растворителя, с другими веществами.
1.1.3. Изотопный состав воды
Вода имеет молекулярный вес равный 18. Однако, не все молекулы воды являются одинаковыми. Часть молекул воды имеет вес 19, 20, 21 и даже 22. Это происходит потому, что некоторые молекулы воды составлены не из обычных атомов кислорода и водорода, имеющих атомный вес 16 и 1 соответственно, а из атомов более тяжелых. Кроме атомов кислорода, имеющих атомный вес 16, в воде обнаружены атомы кислорода с весом 17 и 18, которые обозначаются 17О и 18О. Количество «тяжелых» атомов в общей смеси атомов кислорода очень мало и определяется соотношением 16О : 17О : 18О = 3150 : 5 : 1. Для водорода найдены также тяжелые атомы с весом 2 и 3.
 Изотопы водорода распространены на Земле в соотношении: 1Н (протий) 99,9844 %, 2Н (D-дейтерий) 0,0156 %, 3Н (Т- тритий) 3х10-16 %. В гидросфере количество протия (1Н) примерно в 6000 раз больше, чем дейтерия.
Изотопы водорода распространены на Земле в соотношении: 1Н (протий) 99,9844 %, 2Н (D-дейтерий) 0,0156 %, 3Н (Т- тритий) 3х10-16 %. В гидросфере количество протия (1Н) примерно в 6000 раз больше, чем дейтерия.