|
|
|
|
|
Вкладка в разработке Содержание вкладки готовится.
|
|
|
2. Теоретическая часть Изотерма сорбции гигроскопически чистого твердого кристаллического вещества (типа хлорида натрия) имеет вид, приведенный на рис. 1, а изотерма сорбции технического продукта (содержащего гетерогенные примеси) имеет вид, приведенный на рис. 2. Разные примеси с основным веществом образуют эвтонические растворы с разной равновесной относительной влажностью воздуха над собой, поэтому каждая примесь характеризуется своей индивидуальной изотермой абсорбции (рис. 3). текст текст
|
|
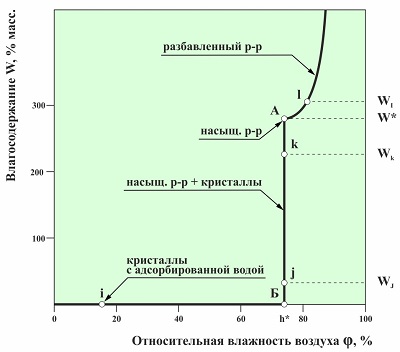 <p>Рис. 1. Изотерма абсорбции паров воды гигроскопически чистым веществом (≥99,99%). В диапазоне относительных влажностей от нуля до точки Б наблюдается только адсорбция паров воды, которая не превышает 0,01 % масс.</p> <p>Точка Б – начало абсорбции паров воды, в которой растворяется вещество, образуя насыщенный раствор (первая микрокапля) на поверхности кристаллов.</p> <p>Точка А – характеризует насыщенный раствор (W* - обратная величина растворимости вещества, h* - гигроскопическая точка вещества), в этой точке растворяется последний микрокристалл вещества.</p>
|
|
|
Рис. 1. Изотерма абсорбции паров воды гигроскопически чистым веществом (≥99,99%). В диапазоне относительных влажностей от нуля до точки Б наблюдается только адсорбция паров воды, которая не превышает 0,01 % масс. Точка Б – начало абсорбции паров воды, в которой растворяется вещество, образуя насыщенный раствор (первая микрокапля) на поверхности кристаллов. Точка А – характеризует насыщенный раствор (W* - обратная величина растворимости вещества, h* - гигроскопическая точка вещества), в этой точке растворяется последний микрокристалл вещества.
|
|
 Рис. 2. Изотерма абсорбции паров воды техническим продуктом (NaCl - 99% и KCl -1%).
|
|
|
Рис. 2. Изотерма абсорбции паров воды техническим продуктом, содержащим NaCl - 99% и KCl -1%. Точки В и Б - характеризуют эвтонический раствор с определенной величиной относительной влажности воздуха (hэ), который содержит жидкую фазу (точка В – первая микрокапля раствора) и две твердых фазы: кристаллы основного компонента и примеси (в точке Б растворяется последний микрокристалл примеси). Точка А/ - характеризует насыщенный раствор основного компонента, содержащего примесь, в котором содержится последний микрокристалл основного компонента. Линия 2 - равновесное влагопоглощение (в диапазоне относительных влажностей воздуха от Б до А/) прямо пропорционально содержанию примеси.
|
|
 Рис. 3. Изотермы абсорбции паров воды образцами хлорида натрия с разными примесями (NaCl-99%+KCl-1%), (NaCl-99%+MgCl2-1%), (NaCl-99%+LiCl-1%).
|
|
 Рис. 4. Изотерма паров воды техническим продуктом.
|
|
|
Рис. 4. Изотерма паров воды техническим продуктом.
|
|
|
1. Абсорбции паров воды реактивом за счет примесей (за счет эвтонического раствора примесей и основного компонента). Изотерма абсорбции начинается с критической относительной влажности воздуха (КОВ), с величин влагосодержания на уровне 0,01% масс. (при более низких относительных влажностях была адсорбция). При влагосодержании примерно 0,01 % уже можно говорить о наличие жидкой фазы в образце, далее абсорбция медленно увеличивается до величин порядка 1 % масс., график изотермы стелется вдоль горизонтальной оси. На некотором небольшом участке изотермы, при относительной влажности воздуха (о.в.в.) ниже на 1 – 5 % о.в.в., чем над насыщенным раствором основного компонента, график изотермы из почти горизонтального переходит в почти вертикальный. 2. Абсорбция паров воды основным компонентом реактива. Почти вертикальный участок изотермы абсорбции характеризуется величинами влагосодержания от нескольких процентов до десятков и сотен процентов. Эта ветвь изотермы абсорбции ограничена растворимостью основного компонента в воде (точнее величиной обратной растворимости вещества) с учетом примесей – точкой А/. 3. Третий участок изотермы, в котором, по мере увеличения относительной влажности воздуха, в точке А/ растворяется последний микрокристалл основного компонента, и далее раствор станет ненасыщенным. В области ненасыщенных растворов другие закономерности абсорбции паров воды от состава реактива, поэтому они не рассматриваются. Если взять образец исследуемого реактива, с изотермой изображенной на рис. 4, высушить его до постоянной массы, то он отобразится некоторой точкой, например, Sd,1, расположенной левее точки КОВ. Если в то же самое вещество добавить несколько капель воды, увлажнить его до 10 – 50 % от его растворимости в воде, то такой насыщенный раствор отобразится точкой на вертикальном участке изотермы, например, точкой Sw,1. Два таких образца, помещенные в герметичную камеру (эксикатор), будут обмениваться влагой. Так как относительная влажность воздуха над увлажненным образцом Sw,1 всегда больше, чем относительная влажность воздуха над сухим образцом Sd,1, между образцами будет происходить гигроскопический процесс: пары воды из бюкса с образцом, характеризуемым точкой Sw,1, будут перемещаться в бюкс с образцом, характеризуемым точкой Sd,1. Если через некоторое время (не доводя процесс до равновесия) прервать процесс, то получим образцы, характеризующимися точками Sd,2 и Sw,2. Увеличение массы изначально сухого образца Wпр будет аналитическим сигналом относительно содержания суммы примесей в пробе. Величина аналитического сигнала будет зависеть от ассортимента примесей и степени их гигроскопичности, а так же от количественного содержания примесей. В связи с тем, что процесс не доводится до равновесия, то по влагопоглощению сухого образа за определённое время можно говорить только о полуколичественной оценке содержания примесей. текст
|
|
|
3. Методика определения При выполнении анализа используются аналитические весы с пределом повторяемости ±0,0001 г, стандартные стеклянные низкие бюксы, стандартный стеклянный эксикатор ≤1,5 л. От анализируемой партии реактива отбирается рабочая проба, которая разделяется на две части по 1 - 10 грамм. Одна часть помещается в пустой взвешенный бюкс и высушивается до постоянной массы. Вторая часть помещается в бюкс, увлажняется деионизированной водой или бидистиллятом до 10 – 20 % от растворимости вещества (если растворимость вещества 50 г /100 г воды, на навеску в 3 г добавляется 0,6 – 1,2 г, или 15 – 30 капель). Капли воды наносятся равномерно по поверхности навески. Бюксы устанавливаются на керамическом вкладыше эксикатора рядом друг с другом, открываются крышки бюксов, закрывается крышка эксикатора, засекается время начала эксперимента. Эксикатор устанавливается при комнатной температуре в закрытом шкафу для защиты от сквозняка и прямых лучей солнца. Через 24 часа открывается эксикатор, закрываются крышки бюксов, бюкс с исходной сухой навеской взвешивается на аналитических весах. Рассчитывается величина влагопоглощения (Wпр, % масс.) сухой навеской за 24 часа. Wпр = (m2 – m1) 100%/( m1 - mб) где m1 - масса бюкса с высушенным образцом до выдержки, г, mб – масса пустого бюкса, г, m2 – масса бюкса с образцом после увлажнения, г. Делается вывод о степени чистоты реактива и содержания в нем суммы примесей, основанием для этого могут быть следующие соображения: а. Если величина влагопоглощения ≤ 0,01 % масс. (не превышает чувствительности взвешивания на аналитических весах), то это дает основание утверждать, что реактив «гигроскопически чистый», весьма вероятно, что содержание основного компонента в реактиве не менее 99,99 % масс. При этом, конечно, надо понимать, что нерастворимые примеси не учитываются. б. Если величина влагопоглощения около 1 % масс. и более, то это говорит о значительном содержании примесей, более 1 %. в. Промежуточные варианты увлажнения можно оценивать, исходя из той же пропорции – сумма гигроскопичных примесей (П, % масс) равна влагопоглощению сухой навески за 24 часа при относительной влажности воздуха, задаваемой насыщенным раствором того же вещества. П = Wпр Характеристика погрешности может быть оценена равной от 100 % отн. и более. Содержание основного компонента (О, % масс.) в партии реактива можно оценить по формуле: О = 100,00 % - Wпр
|
|
|
4. Рекомендации по использованию метода Метод опробован на стабильных растворимых кристаллических неорганических солях (NaCl, KCl) в диапазоне содержания примесей от 3 до 0,001 % масс. Не рекомендуется использовать метод применительно к нестабильным веществам при комнатных условиях (легкогидролизующиеся; кристаллогидраты, не стабильные в условиях сушки и др.). Не рекомендуется использовать высокие бюксы. Нет теоретических ограничений на замену воды другим (органическим) растворителем. Неопределенность метода может быть значительно улучшена, если метод будет валидирован для продукта, получаемого по определенному технологическому процессу, содержащего определенные примеси. Время выдержки может быть сокращено за счет вентилирования воздуха в эксикаторе (Например, вентилятор от компьютера сокращает время эксперимента с 24 до 2 часов). Эксикатор может быть заменен на любую другую герметичную емкость, лучше меньшего объема (не более 0,5 л) текст
|
|
|
Литература Терещенко А.Г. Гигроскопический гравиметрический метод анализа для контроля качества твердых растворимых веществ // Тезисы докладов Третьего съезда аналитиков России, 8-13 октября.2017., г.Москва,: http://rusanalytchem.org/car2017/Publications/2017-Abstracts.pdf 2017. Москва: ГЕОХИ РАН. 2017. С. 84. Anatoly G. Tereshchenko. Application of Hygroscopic Gravimetric Analysis Method in Isopiestic Measurements. Quality Control of Initial Reagents. Journal of Solution Chemistry, March 2019, Volume 48, Issue 3, pp 283–295. https://link.springer.com/article/10.1007%2Fs10953-018-0759-3
|
|
 |
|
|
|
|